化学反应活化能
以下是博文学习网为大家整理的关于化学反应活化能的文章,希望大家能够喜欢!
化学反应活化能篇一:降低化学反应活化能的酶 导学案
第五章 第一节 《降低化学反应活化能的酶》
第一课时酶的作用和本质 学案
【学习目标】
1.学生阅读教材P78,理解细胞代谢的场所、实质及意义。
2.学生阅读教材P78-79“比较过氧化氢在不同条件下的分解”实验,通过课前预习明确实验原理、实验步骤,确保课中小组能够合作完成实验。
3.学生通过进行该实验,学会控制自变量,观察和检测因变量的变化,以及设置对照组和重复实验,同时提高动手操作能力和小组合作能力。
4.学生通过对实验条件和现象的比较,理解酶在细胞代谢中的作用,同时体会酶对细胞内化学反应的顺利进行是至关重要的。
5.学生阅读教材P80的内容,通过对问题串的进一步探究,理解酶作用的机理。
6.学生阅读教材P81-82“关于酶本质的探索”的资料,通过总结各位科学家的观念,归纳和理解酶的定义及本质。
7.学生通过谈谈对科学发展过程的认识,体会科学是在不断的探索和争论中前进的。
【学习建议】
本节课采用教师的过程式教学与学生的探究性学习相结合的方法。课前学生在预习中通过思考,
明确自己的疑惑,并记录在相应位置。课堂中学生通过实验操作,采用观察―思考―分析―讨论―得出结论的方法,重点解决酶的作用机理和酶的本质。
教学中主要采用了实验探究法、观察法、讨论法、总结归纳法。
【重点和难点】
重点:酶的作用、本质。
难点:(1)酶降低化学反应活化能的原理。(2)控制变量的科学方法。
<课前预习区 35min>
【问题探讨】斯帕兰札尼对鹰的消化作用的研究
〖知识扩充〗
1. 消化:在消化道内将食物分解成可以吸收的成分的过程。
2.物理消化:通过牙齿的咀嚼、舌的搅拌和胃的蠕动,将食物磨碎、搅拌并与消化液混合。 3.化学消化:通过各种消化液、消化酶的作用,使食物中各种成分分解为可吸收的营养物质。 阅读课本P78“问题探讨”,根据〖知识扩充〗的提示思考:<4min> 1.将肉块放在笼子里是为了排除________消化的干扰,进而探究鸟类的胃里除________消化外,是否有___________消化。
2.一段时间后,肉块消失了说明胃内_______(有或没有)化学性消化, 使肉块消失了的物质应是_____________________。
学习目标一:酶在细胞代谢中的作用
1.细胞代谢 <课本P780.5min>
概念:______每时每刻都进行着许多_________,统称为细胞代谢。
意义:是________________________的基础。2.实验:比较过氧化氢在不同条件下的分解
要求:认真阅读P78-79所有内容后,再填写学案,切忌断章取义。<5min>
(1)实验原理 <0.5min>
水浴加热
H2O2 H2O + O2
(2P78 1min>选材:新鲜肝脏研磨液
①“新鲜”原因__________________________ ;
②H2O2 酶在细胞内部,本实验使用“研磨液”目的_________________。 (3)方法步骤<课本P79 掌握大致实验步骤2min > 注意:点燃的卫生香放在试管内液面的______,不能触碰到气泡或插到液面以下,原因:_________。 (4)得出结论:
(5)控制变量<课本P79 4mim>
①变量
②除一个因素以外,其余因素都保持不变的实验叫做 ,它一般设置 组和 组。 思考:根据①②总结实验原则:__________,______________ ③思考本实验中的变量:
Ⅰ.自变量是__________,______________,__________ Ⅱ.因变量是________________________
Ⅲ.无关变量有____________________________
Ⅳ.本实验的对照组是_____号试管,实验组是____________号试管。 3.酶的作用机理 <课本P80 4min>
(1)活化能:分子从______转变为的活跃状态所需要的能量。思考问题串:
①加热能加快化学反应速度的原理是加热_______________________
②无机催化剂,酶都可以加快化学反应速度的原理是______________ ③无机催化剂与酶催化效率一样吗?为什么?____________________ (2)意义:使细胞代谢能在__________条件下快速进行。
学习目标二:酶的本质
1.酶本质的探索历程<课本P81-82 8min,注意归纳总结> 1)巴斯德之前:发酵是纯化学反应,与生命活动无关 2)发酵巴斯德提出:发酵与____________有关 争论
李比希认为:发酵与死细胞中的______有关 3)毕希纳:死细胞中的物质和活细胞都能引起发酵
4)萨姆纳:1926年用丙酮提取出了刀豆种子中的_______并证明其化学本质为__________ 5)切赫和奥特曼:发现少数_________也具有催化功能.
【预习检测1】关于酶本质的研究,按时间的先后顺序,排列正确的是( )
①证明了脲酶是一种蛋白质 ②酒精发酵需要活细胞的参与 ③发现少数RNA也具具有生物催化功能 ④人们认识到酿酒就是让糖类通过发酵变成酒精和二氧化碳⑤用不含酵母菌的提取液进行发酵获得成功,证明生物体内的催化反应也可能在体外进行
A.①⑤④②③ B.③④⑤②①C.⑤③④①② D.④②⑤①③ 2.酶的本质:(根据探索历程,进行归纳总结)
(1)定义:酶是______产生的,具有_________作用的________。(2)本质:绝大多数酶是_______,少数酶是_______。 【预习检测2】酶的基本组成单位是 ( )
A.氨基酸 B.核苷酸C. 氨基酸或核苷酸D.甘油和脂肪酸
我的疑惑:
<课中进行区>
学习目标一:酶在细胞代谢中的作用
1.细胞代谢场所:________
实质:各种___________的总称 2.实验:比较过氧化氢在不同条件下的分解 (1)实验操作中注意问题
①滴入肝脏研磨液和FeCl3溶液时,不能共用一个吸管。否则滴入的FeCl3溶液中会含少量肝脏研磨液而影响实验结果的准确性。
②H2O2有腐蚀性,使用时要小心,不要触及皮肤。
(3)根据实验现象,解决以下问题:
①1号与2号试管现象相比,说明________能促进H2O2 的分解速率。 ②1号和3号对照说明:___________能促进H2O2 的分解速率。 ③1号和4号对照说明:___________能促进H2O2 的分解速率。 由①②③可以得出结论是:酶具有_____作用。
④3号和4号对照,_____号试管反应速率快,说明:______________________________由此可以得出结论:
_____比_________催化效率高,原因是_______________________________________ (4)酶的作用机理 思考问题串:
Ⅰ.加热能加快化学反应速度的原理是加热_________________________________________
Ⅱ.无机催化剂,酶都可以加快化学反应速度的原理是_______________________________ Ⅲ.无机催化剂与酶催化效率一样吗? _____________为什么?________________________ 【牛刀小试1】
用图中所给字母回答下列问题
①图中表示无机催化剂催化反应进行所需要的活化能是______②图中表示酶催化反应进行所需要的活化能是______
③体现出酶比无机催化剂降低活化能作用更显著的是_______
学习目标二:酶的本质
1.设计实验证明某种酶是蛋白质。
2. 设计实验证明某种酶是RNA。
本节小结:
自变量
因变量
活化能
蛋白质RNA
【课后练习】
1.下列图中,①表示有酶催化的反应曲线,②表示没有酶催化的反应曲线, E表示酶降低的活化能。正确的图解是
( )
2.细胞内酶合成的主要场所是 ( )
A.线粒体B.高尔基体 C.核糖体 D.内质网
3.用某种物质处理细胞,处理后,该细胞的膜仅具有自由扩散的运输方式,则处理该细胞的物质最可能是 ( )
A.淀粉酶 B.蛋白酶 C.脂肪酶 D.生长素
4.催化脂肪酶水解的酶很可能是 ( )
A.肽酶B.蛋白酶C.脂肪酶 D.淀粉酶
5.甲、乙两种酶用同一种蛋白酶处理,酶活性与处理时间的关系如右图所示。下列分析错误的是 A.甲酶能够抵抗该种蛋白酶降解 B.甲酶不可能是具有催化功能的RNA C.乙酶的化学本质为蛋白质
D.乙酶活性的改变是因为其分子结构的改变
化学反应活化能篇二:5.1降低化学反应活化能的酶教案
第5章 细胞的能量供应和利用
第1节 降低化学反应活化能的酶
一、教学目标
1、 知识与技能目标
(1)说出细胞代谢的概念。
(2)说明酶在细胞代谢中的作用。
2、 过程与方法目标
(1)通过有关的实验和探索,学会控制自变量,观察和检测因变量的变化,及设置对照组和重复实验
(2)提高学生观察、分析、判断的思维能力,提高学生的实验操作能力。
3、 情感态度与价值观目标
(1)通过有关的实验和探索使学生体验实验成功的喜悦,并通过教师的引导使学生领悟科学实验的基本方法。
(2)培养学生的探索精神和合作意识。
二、教学重点和难点
1、教学重点
(1)酶的作用
(2)控制变量的科学方法
2、教学难点
(1)酶降低化学反应活化能的原理
(2)控制变量的科学方法
三、教学过程
1、导入
学习细胞器时,我们了解到在很多细胞器上都发生着化学反应。细胞产生能量、合成养料以及进行自我更新等等生理活动,都完全依赖细胞内发生的生物化学反应。细胞内全部的化学反应的总称就是细胞代谢。细胞内每时每刻都在进行着化学反应,这些反应如何能够高效地进行呢?那是因为有催化剂的存在。但是很多化学反应往往需要高温高压的条件,但生物体内是一个常温常压的状态,如何解决这个矛盾呢?就需要一种特殊的催化剂。酶就是生物体内的催化剂。
让我们结合资料看看科学家是如何发现酶的存在的。介绍教材P78斯帕兰扎尼的实验: 1773年,意大利科学家斯帕兰扎尼将肉块放入小巧的金属笼内,然后让鹰把小笼子吞下。过一段时间后,把小笼子取出,发现肉快消失了。
引导学生分组讨论如下问题:(请学生讨论并展示,教师予以解释和评价)
1.为何要将肉块放在笼子中?(排除了胃对肉块的物理性消化。)
2.对肉起消化作用的是什么物质?(一定是某种物质进入到笼子中,使肉分解。)
3.在实验室中能否也让肉分解?能的话需要怎样的条件?(能。需要高温、高压、强酸或强碱等剧烈条件。)
当时斯帕兰扎尼做过这个实验后他并不清楚起消化作用的物质是什么,但他的研究却为人们研究提供了方法和思路。1836年,德国科学家施旺从胃液中提取出了消化蛋白质的物质,解开胃的消化之谜。这种物质就是酶。本节课我们先来学习酶的作用与本质,请大家注意思考本节聚焦的重点问题。
2、展示
分小组展示学案中[阅读要求及检测]部分,检验学生阅读课本及预习的效果,教师给予
评价。
3、要点与典型例题精讲
一、酶在细胞代谢中的作用
细胞中每时每刻都进行着许多化学反应,统称为细胞代谢。我们书上举了一个例子来说明酶的作用和作用特点。那就是对过氧化氢这种物质的分解。人体的新陈代谢除了生成人体需要的物质,也会有一些对人体有害的副产品产生,比如水系化合物在氧化时会产生过氧化氢。过氧化氢H2O2俗称?(双氧水)过氧化氢是一种强氧化剂,在人体内堆积的话会造成DNA损伤,并且加速人体的衰老进程。
性质:过氧化氢可自发分解生成水和氧气
2 H2O2→ 2 H2O + O2
这个反应在自然条件下反应的比较缓慢,但细胞中具有的物质却可以加速这个反应。 请学
(1) 实验中比较过氧化氢在不同条件下的分解,这里的“不同条件”指哪些?
(2号:90度水浴加热;3号:加入3%的氯化铁;4号:加入20%肝脏研磨液)
(2) 自变量、因变量、无关变量各是什么?
(自变量:实验过程中可以人为改变的变量。本实验中氯化铁溶液和肝脏研磨液。 因变量:随着自变量的变化而变化的变量。本实验中过氧化氢分解速率。
无关变量:除自变量外,其他可能对实验结果造成影响的因素。加入试剂的量;实验室的温度;氯化铁和肝脏研磨液的新鲜程度等。无关变量是误差的产生根源,我们要尽量减少无关变量对实验的影响,因此尽量①所有用生物材料要相同②所用实验器具要相同③所用实验试剂要相同④所用处理方法要相同)
(2) 为什么要设计四组实验,1号组有什么作用?
(除了一个因素以外,其余因素都保持不变的实验叫做对照实验。四组实验符合对照实验的要求,其中1号就是对照组)
教师可在教室或实验室进行实验操作,学生注意观察不同的条件下,过氧化氢的分解速率如何。记录现象并进行讨论:
1、 与1号试管相比,2号出现什么不同的现象?这一现象说明什么?
(2号放出的气泡多,说明加热能促进过氧化氢的分解,提高反应速率。)
2、 在细胞内能通过加热提高反应速率吗?
(不能)
3、3号和4号未经加热,也有大量气泡产生,这说明什么?
(说明FeCl3中的Fe3+和新鲜肝脏中的过氧化氢酶都能加快过氧化氢分解的速率。) 4、3号与4号相比,4号试管中的反应速率快?这说明什么?为什么说酶对于细胞内化学反应顺利进行至关重要?
(说明过氧化氢酶的催化速率比Fe3+高效得多。细胞内每时每刻都在进行着化学反应,这些化学反应需要在常温、常压下进行,只有酶能够满足这样的要求进行催化,所以说酶对于细胞内化学反应的顺利进行至关重要。)
既然酶对于细胞内化学反应的顺利进行至关重要,为什么酶可以在常温常压下高效地催化化学反应进行呢?我们可以先了解加热促进反应的原理,加热促使过氧化氢分解是因为加热使过氧化氢分子得到能量,从常态转变为容易分解的活跃状态。分子从常态转变为容易发生化学反应的活跃状态所需要的能量称为活化能。
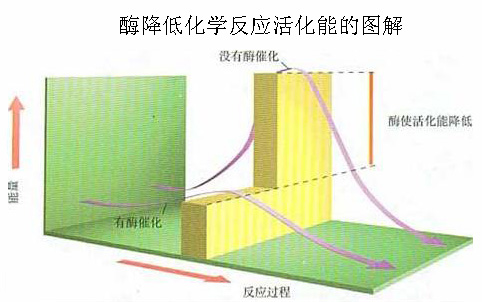
过氧化氢酶促使过氧化氢分解并未供给过能量,而是降低了过氧化氢分解反应的活化能。推而广之,酶促使反应进行,原因是酶能够降低化学反应活化能。对于这句话的理解可以阅读第80页内容,注意图5-1和5-2。
分子从常态转变为容易发生化学反应的活跃状态所需要的能量。活化能越低,反应发生的速率越快。如果把发生化学反应比喻为驾驶汽车翻越一座高山,加温加压相当于加大油门,而催化剂则相当于帮司机找到一条穿山隧道。这就是催化剂所体现的优越性。而同无机催化剂相比,酶降低活化能的作用更显著,效率更高。
二、酶的本质
酶究竟是什么物质呢?我们现在已经知道了大多数的酶是蛋白质。但是酶的本质是怎样被揭示出来的呢?让我们共同来回顾这一段科学发展史。请阅读第81页资料分析,填写第82页基础题第一题。再尝试回答讨论中的5个问题。
1、巴斯德和李比希的观点各有什么积极意义?各有什么局限性?
(巴斯德认为发酵与活细胞有关是合理的,但是认为发酵是整个细胞而不是细胞中的某些物质在起作用是不正确的;李比希认为引起发酵的是细胞中的某些物质是合理的,但是认为这些物质只有在酵母细胞死亡并裂解后才能发挥作用是不正确的。)
2、科学发展过程中出现争论是正常的。试分析巴斯德和李比希之间出现争论的原因是什么,这一争论对后人进一步研究酶的本质起到了什么作用?
(巴斯德是微生物学家,特别强调生物体或细胞的作用;李比希是化学家,倾向于从化学的角度考虑问题。他们的争论促使后人把对酶的研究的目标集中在他们争论的焦点上,使科学研究更加有的放矢。)
3、从毕希纳德实验可以得出什么结论?
(毕希纳的实验说明,酵母细胞中的某些物质能够在酵母细胞破碎后继续起催化作用,就像在活酵母细胞中一样。)
4、萨姆纳历时9年才证明酶为蛋白质,你认为他成功的主要原因是什么?
(萨姆纳历时9年用正确的科学方法,坚持不懈、百折不挠的科学精神,将酶提纯出来。成功属于不畏艰苦的人。)
5、请给酶下一个完整的定义。
(来源、功能、化学本质。酶是活细胞产生的具有催化作用的有机物,其中绝大多数酶是蛋白质,少数是RNA等。)
4、训练
请同学完成学案中[自主训练]的前6道选择题,并请每组派代表公布答案并给予简要解释。
5、总结
一、 酶在细胞代谢中的作用
1、 作用:催化化学反应
实验:比较过氧化氢在不同条件下的分解
控制变量:自变量 因变量 无关变量
2、 原理:降低化学反应的活化能
二、 酶的本质
1、 对酶本质的探索历程
2、 酶的本质:酶是活细胞产生的具有催化作用的有机物,其中绝大多数酶是蛋白质,
少数是RNA等。
6、作业
完成习题本中本节中的选择题必作题。
化学反应活化能篇三:反应速率常数与活化能
大学化学结课论文
反应速率常数与活化能
院 (系) 专 业 学 生 学 号 班 号指导教师日 期
哈尔滨工业大学
2014年12月
反应速率常数与活化能
摘要:反应速率常数与活化能是大学化学的一个重要部分,反应速率常数与活化能的测定的实验通过对H202和酸性KI的反应的研究与计算,得到了反应的反应速率常数和活化能。本文主要对此实验进行分析,并对反应速率常数和活化能进行简要介绍。 关键词:活化能;反应速率;实验。
Determination of the reaction rate constant and
activation energy
Abstract: the reaction rate constant and activation energy is an important part of college chemistry, and the determination of reaction rate constant and activation energy of experiment through reaction of H_2 0 _2 and acidic KI research and calculation, get the reaction rate constant and activation energy of the reaction. In this paper, this experiment is analyzed, and the reaction rate constant and activation energy are briefly introduced. Key words: activation energy; The reaction rate. The experiment.
反应速率常数与活化能的测定的实验,利用H202和酸性KI的反应,通过一系列的实验观察与计算,研究了反应速率的影响因素,计算得到了反应速率常数与活化能。 一、实验简介 1、实验目的:
1)学会测定化学反应速率常数和活化能; 2)了解温度对反应速率的影响。 2、实验原理:
反应方程式
1)I?+H202 IO?+H20 2) I?+IO?+2H+ I2+H20
2?2?
3) I2+2S2O3 2I?+S4O6
4) I2+淀粉 蓝色 速率常数表达式:k=
2.303t
lg0
ct
c
式中 c0:H202在时间t=0时的浓度; ct:H202在时间t时的浓度。
利用阿累尼乌斯公式:lgk2=2.303R(T?T)
1
1
2
kE11
式中 k1、k2――在温度T1、T2时的反应速率常数; E――反应的活化能; R――理想气体常数。 3、实验过程
1)酸性碘化钾溶液的配制
取250ml容量瓶,加入30ml 0.4mol?L?1KI溶液,加水到容量瓶体积的2/3处后,再加入15ml 3mol?L?1 H2SO4及3ml淀粉溶液,加水稀释到刻度,摇匀。将全部溶液倒入1000ml的烧杯内。
2)室温时H202反应速率常数的测定
在装有反应液的烧杯中放入一磁子,将烧杯放在磁力搅拌器上搅拌。用注射器取1ml 0.1000mol?L?1 Na2S2O3溶液注入烧杯中,然后用移液管吸取10ml
0.1000mol?L?1 H202溶液加入此烧杯中,反应开始进行。当溶液第一次出现蓝色时,随即启动电子秒表,并立即加入1ml Na2S2O3溶液(注意:按表和注入要同时进行)。当蓝色第二次出现时,利用电子秒表的取样功能,记录时间数据,同时再加入1ml Na2S2O3溶液,以此类似,每当蓝色出现时,均计时并加入1ml Na2S2O3溶液,直到记录5次时间数据为止。 3)高于室温10摄氏度时反应速率常数的测定
同前配制溶液。将盛有反应液的烧杯放到恒温水浴上加热,当加热到高于原始溶液温度10摄氏度时,将烧杯移至磁力搅拌器上搅拌。由于在高温时,反应速率很快,反应时间很短,而所用反应溶液又较多,所以在测定过程中,温度下降不多,可以满足测量精度。 4、实验结果
由实验数据可以看出,温度越高,反应速率越快。而且活化能不是一个定值,测量过程中也存在误差,测量结果必然存在一定的误差。 二、理论简介与分析 1、反应速率常数
反应速率常数即化学反应进行的快慢。用单位时间内反应物浓度的减少或生成物浓度的增加量来表示。
可通过实验测定。除了反应物的性质以外,浓度、温度和催化剂也是影响反应速率的重要因素。气体还有压强。
气体反应的快慢还与压力有关。增加反应物的浓度,即增加了单位体积内活化分子的数目,从而增加了单位时间内反应物分子有效碰撞的次数,导致反应速率加快。提高反应温度,即增加了活化分子的百分数,也增加了单位时间内反应物分子有效碰撞的次数,导致反应速率加快。使用正催化剂,改变了反应历程,降低了反应所需的活化能。 2、活化能
活化能是指化学反应中,由反应物分子到达活化分子所需的最小能量。以酶和底物为例,二者自由状态下的势能与二者相结合形成的活化分子的势能之差就是反应所需的活化能,因此不是说活化能存在于细胞中,而是细胞中的某些能量为反应提供了所需的活化能。
化学反应速率与其活化能的大小密切相关,活化能越低,反应速率越快,因此降低活化能会有效地促进反应的进行。酶通过降低活化能(实际上是通过改变反应途径的方式降低活化能)来促进一些原本很慢的生化反应得以快速进行。 3、过氧化氢与酸性碘化钾反应的动力学
H202与酸性KI反应的化学方程式:
H2SO4+KI+H202=2H2O+I2+K2SO4
离子方程式:
2H++2I?+H202 2H2O+I2
在KI的酸性溶液中,加入一定量的淀粉溶液和Na2S2O3标准溶液,然后一次加入一定量的H202溶液。有如下反应:
1)I?+H202 IO?+H20反应很慢 2) I?+IO?+2H+ I2+H20反应很快
2?2?3) I2+2S2O3 2I?+S4O6 反应很快
4) I2+淀粉 蓝色 反应很快 反应速率可以写成
?
d H202
=k′ H202 I? =k[H202] t
dc? =k dt c00
ct
?ln=kt
ct
其中k=k′( I?),上式积分得
2.303lg
即:k=
2.303t
ct
=kt 0
lgc0
t
c
再根据阿累尼乌斯公式lg
三、实验误差分析 1、温度的影响
k2k1
=
E
2.303RT1
(?),即可求出活化能。
T2
11
温度会对化学反应的速率产生影响,在这次实验中,第二组高于常温10摄氏度,在测量过程中处于室温条件下,反应溶液的温度会不断下降,这会对实验产生影响,但影响过小可以忽略不计。
温度本身对化学反应速率也有影响,一般情况是温度越高,反应速率越快。温度越高,分子运动越剧烈,分子碰撞机会越多,越容易发生反应,反应速率越快。 2、活化能本身的测定
活化能不是一个定值,测量过程中也存在误差,测量结果必然存在一定的误差。但在精度要求不高的情况下,这种实验方法求出的活化能相对来讲还是比较精确的。 四、反应速率常数与活化能研究的意义
使反应速率加快.在化工生产中,常控制反应条件来加快反应速率,以增加产量.有时也要采取减慢反应速率的措施,以延长产品的使用时间。化学反应速率与其活化能的大小密切相关,活化能越低,反应速率越快,因此降低活化能会有效地促进反应的进行。酶通过降低活化能(实际上是通过改变反应途径的方式降低活化能)来促进一些原本很慢的生化反应得以快速进行。
活化能是指化学反应中,由反应物分子到达活化分子所需的最小能量。阿仑尼乌斯发现化学反应的速度常数k和绝对温度T之间有
d(lnk)dt
=RT2的关系。这里的E就是活化能。假若
E
相关热词搜索:化学反应 活化 化学反应速率与活化能 降低化学反应的活化能

